PICK UP!
2025.01.31
テクノロジーとバイオロジーの両輪で、最先端研究を展開~老化メカニズム解明や新規診断・治療技術の開発へ~
順天堂大学大学院医学研究科生化学・生体システム医科学の洲﨑悦生主任教授の研究室では、「生体組織の3次元解析技術の開発とがん創薬・臨床病理学への応用」「老化関連疾患や老化の謎を解き明かすバイオロジー研究」に取り組んでいます。テクノロジーとバイオロジーという2つの研究領域を両輪に、世界レベルの成果を多数あげている洲﨑先生に、最先端の取り組みについて伺いました。
所属メンバーの多彩な専門分野が生み出す研究室のオリジナリティ
――洲﨑先生の研究室では、どのような研究を行っているのでしょうか。
一言でいうと生物の最も基本的な機能単位である細胞について研究しています。「多細胞生物はどのような細胞から構成され、機能しているのか。また細胞に異常が起こるとどんな疾患が生じるか、それらの疾患に対してどのように新しい治療法を開発するか。」ということが主眼です。私たちの研究室では、とくに老化関連疾患(がん、心血管疾患、神経変性疾患)について注目しており、対象臓器のすべての細胞を3次元で観察して、疾患や老化で細胞社会の状態がどのように変化するかを調べ、データサイエンスやAIなども駆使してメカニズム解明や創薬研究を進めています。そして、この一連の工程を可能にするためのテクノロジーを研究室内で開発しています。研究のために技術を開発し、開発した技術を研究に使用する、という両輪が研究室の重要な方向性です。

――研究室の特徴はありますか。
医学部としては珍しく、研究室内に顕微鏡を開発できる環境を整備しており、独自の計測技術を開発し、研究に役立てているという点です。特に私たちが開発した高度な顕微鏡技術などの生体計測・解析技術は、研究を進めるうえでは欠かせません。また、メンバーの専門も多彩で、疾患生物学、顕微鏡工学、進化生物学、データサイエンスなどの各分野で経験豊富な研究者が、それぞれの強みを活かした研究を進めています。工学、化学、情報学などの多岐にわたる専門家との共同研究も多数行っています。この多様性が、テクノロジーとバイオロジーの2つの研究領域を同時に進める原動力です。
臓器・組織を透明にして、3次元でまるごと観察
~独自に開発した臓器・組織の3次元解析技術~
――開発したテクノロジーについて教えてください
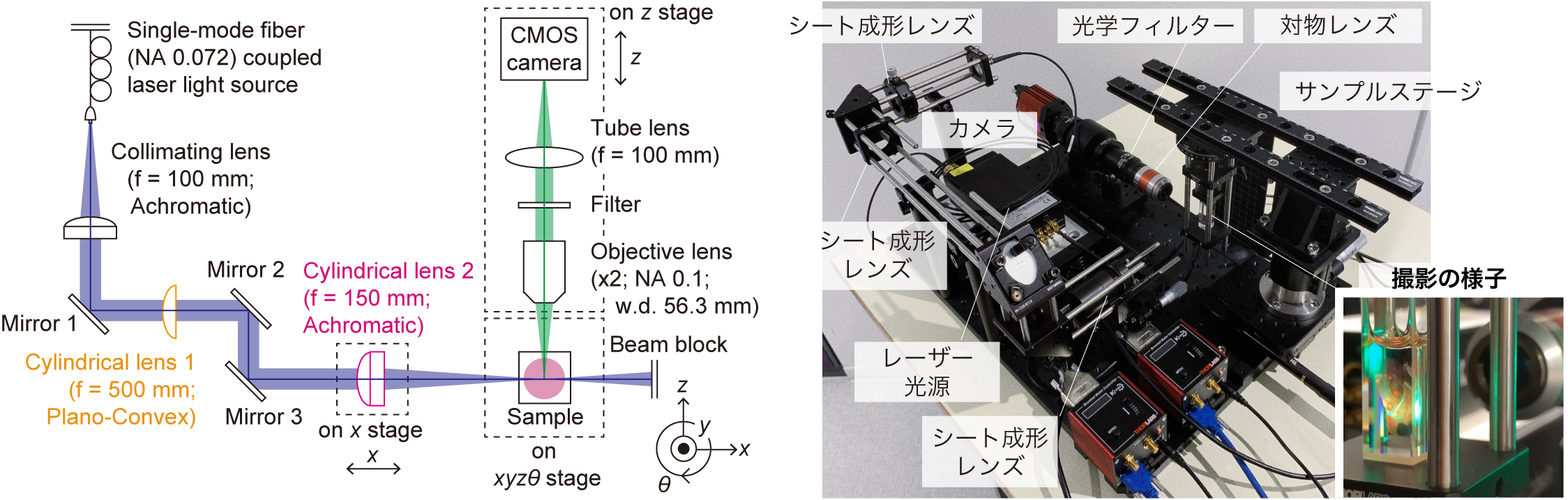
研究に合わせて最先端の技術開発を推進しており、代表的なものは組織透明化とライトシート顕微鏡です。私たちの細胞解析の研究分野を「空間オミクス」といいますが、ここでは3次元で全細胞の「空間的情報」と「分子情報」を網羅的に取得します。3次元になることで、精度や客観性が向上し、立体的に細胞間の位置関係や相互作用についても解析できるので、組織構造についてより深く知ることができます。この3次元解析を可能にするのが組織透明化技術とライトシート顕微鏡の高度な組み合わせです。
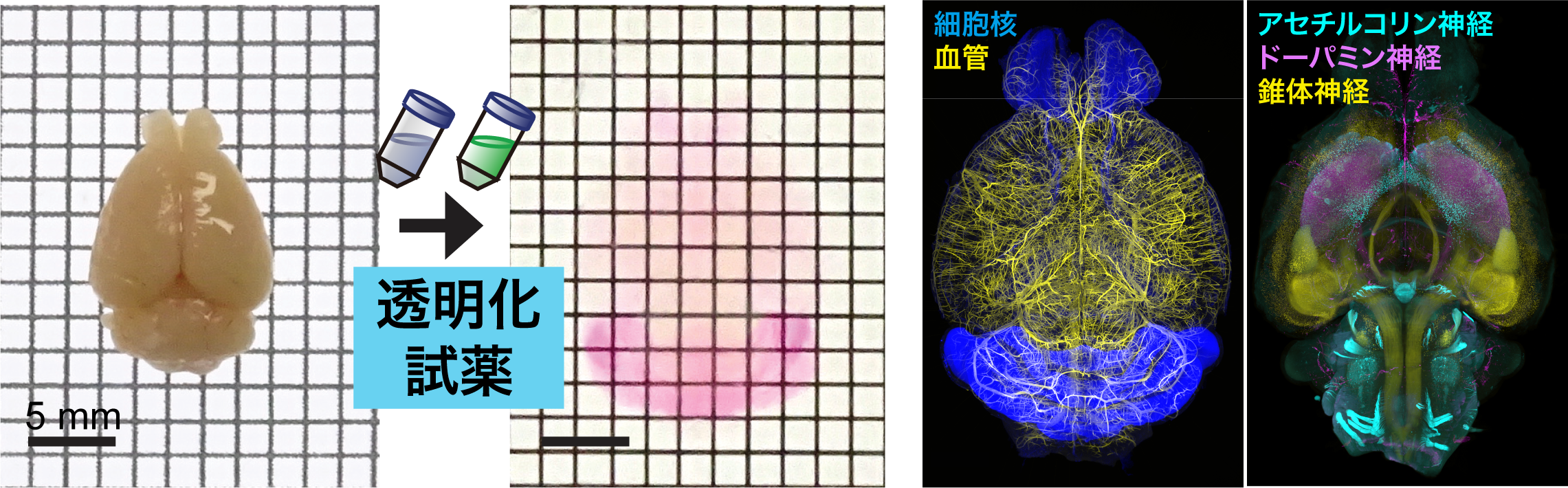
実際には、臓器や組織を光が通るように透明にしたうえで、観察対象となる血管や神経細胞などが光るように空間を均一に染色します。そうして透明化した組織サンプル全体を、ライトシート顕微鏡で連続的にスキャンし、3次元画像化(=3次元イメージング)させています。組織や細胞を3次元で画像化するために私たちが開発した技術は、「CUBIC」という名称で発表しました。CUBICで使用する透明化試薬や染色試薬は製品化し、社会実装も進めています。
――開発にあたって苦労したことは何ですか?
高度な組織透明化の実現と3次元の組織染色技術開発です。ライトシート顕微鏡を使った3次元の観察には、透明化が必須なので、どれだけ透明度を上げられるかが肝でした。高度な透明化を実現するため、私や私の同僚・大学院生が膨大な量の化合物を調査・測定しました。これらの努力が透明化技術の開発に大きく役に立ちました。CUBIC試薬は、現存の透明化手法の中で最も効率の高い透明化試薬の一つです。しかも、従来の透明化手法のように有機溶剤を使う必要がないため、高校生が自由研究で使用できるくらい安全かつ簡易的です。
また、染色技術の開発にもかなりの時間を費やしました。一般的な方法では表面しか染まらないところ、3次元的に組織の中まで均一に染めるのはとても難しく、最初のプロトコルが完成するまでに要した時間は透明化技術の倍の6年くらいかかりました。現在でも性能向上のための開発を進めています。
――これらの技術を用いた研究成果にはどのようなものがありますか。
CUBIC技術は世界中の研究室で使われています。代表的な研究成果としては、神経科学分野が多いです。例えば、実験動物の脳を3次元でまるごと観察することで睡眠を解析し睡眠-覚醒リズムに重要な神経細胞の働きを調べる研究などがあります。また最近では、がん研究や発生学研究などでも盛んに使用されるようになってきています。
特に、近年私たちの研究室で行っているのは、がん創薬と臨床病理学検査*1の3次元化です。がん創薬研究では、脳腫瘍の患者さんから採取したがん細胞からがんオルガノイド(幹細胞を立体的に培養して創り出すミニチュア臓器)を作製し、薬のスクリーニング*2などを進めようとしています。私たちが開発した全細胞解析技術を使うと、薬を使用した際のオルガノイド全体の形の変化を高感度に検出できるため、薬効の度合いをかなり高精度で判定できます。
*1病理学検査…採取した組織や細胞を顕微鏡で観察して病変の性質や悪性度を調べる診断方法
*2スクリーニング…大量のものを検査して、条件に合うものを選び出す研究手法。
病理の世界で「3次元病理」を世界標準に
――3次元病理について教えてください。
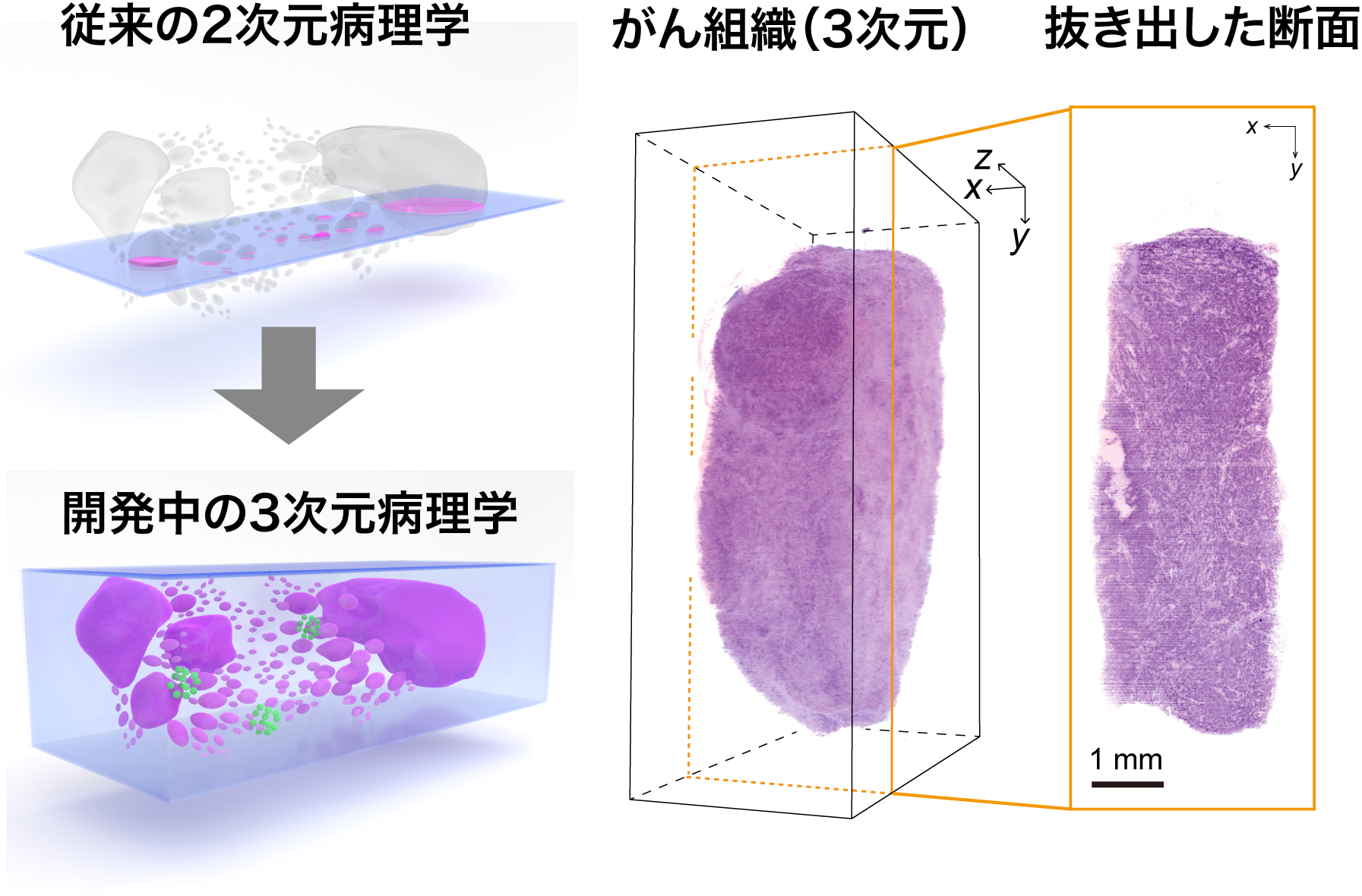
文字通り、病理学検査を3次元で行うことです。現在の病理学検査では、組織を数マイクロメートルの薄い切片にして2次元で調べることが一般的なので、生体組織が本来有する3次元構造を反映できません。病理医の主観が多少なりとも診断結果に影響します。例えば、世界のトップエキスパートである18人の肺がん病理の専門家が肺がんの病理スライドを診断した結果を比較したレポートでは、診断結果にかなりのズレがあることが明らかになりました。
CUBIC(3次元)技術を病理に応用して「3次元病理」にすることで、組織の情報をより網羅的かつ客観的に捉えられるので、病理医ごとに異なる診断結果の差が少なくなり、病理の世界を大きく前進させることになるでしょう。今、3次元病理は世界的にもかなり注目度の高い研究領域で、多くのグループが参入しようとしていますが、透明化技術、解析技術、さらに顕微鏡開発まで行えるグループはまだまだ少ないのが現状です。私たちはその全てにおいて実績がありますから、その強みを活かす応用先の一つが3次元病理です。
――3次元病理において今やろうとしているのはどんなことですか。
病理医や臨床検査技師が日常的な病理診断作業と並行してできるような、臨床病理検査での利用に特化した透明化・染色プロトコルやライトシード顕微鏡の改良版を開発中です。本格的な臨床現場での普及を目指すならば、装置やメソッドを開発して終わりではなく、3次元病理の世界規格を作ることから考えていかなければなりません。
不老生物ヒドラを使って老化を研究
――「老化」の研究について教えてください。
老化をメインテーマに、老化関連疾患であるがんや心血管疾患、神経変性疾患などについての研究に加えて、老化の根本的な原因を解明する研究に取り組んでいます。老化研究ではいくつかアプローチ法がありますが、私たちは不老不死生物だとされているヒドラ(クラゲやイソギンチャクの仲間である刺胞動物)を使って、老化を引き起こす原因となるものを見出そうとしています。
まずは遺伝子改変ヒドラを作り、ヒドラに老化を誘導(再構成)することを考えています。老化したヒドラと老化しないヒドラを比較して、その違いを探っていきたいと考えています。老化の原因となる細胞を明らかにするために、ヒドラの全身全細胞を使った解析を行える新しい技術を開発中です。遺伝子改変ヒドラを作製する技術も重要な開発項目です。

――ヒドラを使うことのメリットはなんでしょうか。
ヒドラの細胞は5万個から10万個程度で、顕微鏡で全ての細胞を観察することができます。老化研究によく使われる不老モデル動物としてはハダカデバネズミもいますが、ネズミは飼育が大変ですし、老化因子を探索するとなると数百単位の集団での表現型を調べる必要があるので、スペースやコストの問題から見てもヒドラが最適だと私たちは考えています。
楽しくなければ、研究は続かない!
――研究者としての目標はなんですか。
リタイアするまでに老化するヒドラを作りたいです。そもそも遺伝子改変が難しいヒドラで遺伝子改変を実現して、ヒドラを老化(再構成)させることができたら、ノーベル賞級の研究成果といえるのではないでしょうか。たとえ老化ヒドラができたとして、それがゴールだとは思っていません。ヒドラ老化によって老化の本質が見えてきてからが本番で、その成果をヒトに応用していきます。老化因子をターゲットとした治療薬を開発することで、老化に関係する疾患の治療や健康寿命の延伸に貢献したいと思っていますし、私たちが開発してきた3次元病理や薬剤スクリーニングなどのテクノロジーは、老化研究の成果を還元することにも活きてきます。

――ラボ運営や人材育成で大事にしていることはありますか。
楽しくないとサイエンスは続かないですから、「みんな楽しく」ですね。研究はとてもクリエイティブな行為ですから、チームリーダーとしての私の重要な役割の一つは、メンバーが最もクリエイティビティを発揮できる環境を準備することだと考えています。研究を通じていろんなものが見えてきて、メンバーは大きく成長しますから、臨床やまったく別の道に進むなど、最終的に別の道を選んだとしても、みんなが幸せになればという思いでラボを運営しています。
――洲﨑先生の研究のモチベーションを教えてください。
研究のモチベーションは、「面白い」に尽きます。だからといって、面白ければ何でもやるというスタンスではなく、なにが本質的に重要か、研究する価値があるかを深く検討して、それぞれのプロジェクトを立案しています。また、成果につながるまでのタイムスケールや、テクノロジー・バイオロジーなどの性格で割り振り、研究室全体のプロジェクトポートフォリオのバランスが取れるように腐心しています。これからも私たちの強みである「細胞を網羅的に全部見る」ということに軸を置いて、基礎研究からビジネス化による社会実装まで、幅広く戦略的に研究を展開していきます。



